Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (16)
Más de fabianchopinto
Más de fabianchopinto (20)
Multifasico
- 3. Reacomodando términos: De manera similar para el agua:
- 4. Para el caso del gas: Gas libre Gas disuelto en aceite Gas disuelto en agua
- 7. Implícito en Presión Explícito en Saturación Método IMPES
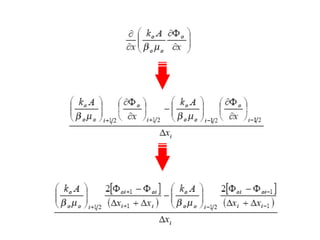
- 8. Implícito en Presión Explícito en Saturación Apróximando cada término interno:
- 9. Si asumimos que la Pc es constante